L’intestin et le cerveau sont intimement liés. D’ailleurs, l’intestin est surnommé « le deuxième cerveau », notamment car il possède le plus de neurones après le cerveau et la moelle épinière.
Dans une étude publiée le 23 octobre 2019 dans la revue Nature, des chercheurs révèlent avoir découvert les premiers indices sur l’influence de la santé intestinale sur la santé du cerveau.
En effet, de nouveaux processus cellulaires et moléculaires sous-jacents à la communication entre les bactéries intestinales et les cellules cérébrales ont été décrits pour la première fois par des scientifiques.
Les altérations du microbiote influencent l’activité neuronale
Au cours des deux dernières décennies, les scientifiques ont observé un lien clair entre les troubles auto-immuns et diverses affections psychiatriques.
Par exemple, les personnes atteintes de maladies auto-immunes telles que les maladies inflammatoires chroniques de l’intestin (MICI), le psoriasis et la sclérose en plaques (SEP) peuvent également présenter un microbiote intestinal affaibli et souffrir d’anxiété, de dépression et de troubles de l’humeur.
Les risques génétiques pour les troubles auto-immuns et les troubles psychiatriques semblent également être étroitement liés.
Cependant, il n’était pas encore précisément connu comment la santé de l’intestin affecte la santé du cerveau.
Les organismes multicellulaires ont co-évolué avec des consortiums complexes de virus, de bactéries, de champignons et de parasites, appelés collectivement microbiote.
Le microbiote est l’ensemble des micro-organismes – bactéries, virus, parasites, champignons non pathogènes, dits commensaux – qui vivent dans un environnement spécifique. Dans l’organisme, il existe différents microbiotes, au niveau de la peau, de la bouche, du vagin… Le microbiote intestinal est le plus important d’entre eux, avec 1012 à 1014 micro-organismes : 2 à 10 fois plus que le nombre de cellules qui constituent notre corps, pour un poids de 2 kilos !
INSERM

Chez les mammifères, des modifications de la composition du microbiote peuvent influer sur de nombreux processus physiologiques (développement, métabolisme, fonction des cellules immunitaires) et sont associées à une susceptibilité à de multiples maladies.
Les altérations du microbiote peuvent également moduler les comportements de l’hôte, tels que l’activité sociale, le stress et les réactions liées à l’anxiété, liés à divers troubles neuropsychiatriques.
Cependant, les mécanismes par lesquels le microbiote influence l’activité neuronale et le comportement de l’hôte restent mal définis.
Dans cette étude, les chercheurs montrent que la manipulation du microbiote chez des souris adultes traitées aux antibiotiques ou sans germes entraîne des déficits importants dans l’apprentissage de l’extinction de la peur.
Aussi, l’analyse a identifié quatre métabolites qui étaient significativement régulés négativement chez des souris sans germe et qui seraient liés à des troubles neuropsychiatriques chez l’homme et chez la souris, suggérant que les composés dérivés du microbiote pourraient affecter directement le fonctionnement et le comportement du cerveau.
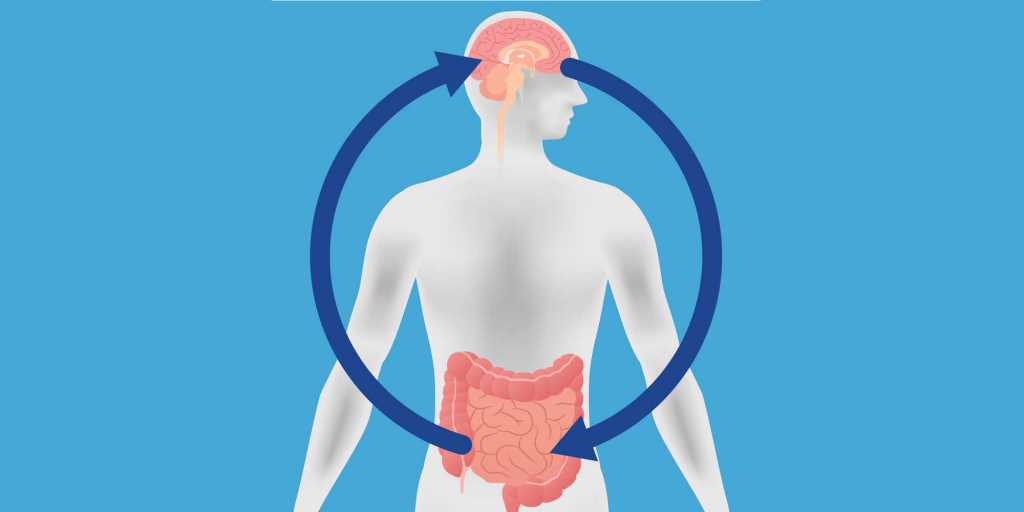
Mécanismes de communication de l’intestin et du cerveau
Cette étude fournit de nouvelles informations sur les mécanismes de communication de l’intestin et du cerveau au niveau moléculaire.
Jusqu’alors personne n’a encore compris comment les maladies intestinales inflammatoires et d’autres affections gastro-intestinales chroniques influent sur le comportement et la santé mentale.
Grâce à cette étude, « le début d’une nouvelle façon de comprendre la situation dans son ensemble apparaît », expliquent les auteurs.
Pour l’étude, les chercheurs ont utilisé des modèles de souris pour comprendre les changements qui se produisent dans les cellules du cerveau lorsque le microbiote intestinal s’épuise.
Les souris traitées avec des antibiotiques pour réduire leurs populations microbiennes ou qui étaient élevées pour être exemptes de germes ont montré une capacité significativement réduite à apprendre qu’un danger menaçant n’était plus présent.
Pour comprendre la base moléculaire de ce résultat, les scientifiques ont séquencé l’ARN dans des cellules immunitaires appelées microglia (cellules microgliales) situées dans le cerveau.
Ils ont aussi découvert qu’une altération de l’expression des gènes dans ces cellules joue un rôle dans le remodelage de la façon dont les cellules du cerveau se connectent au cours des processus d’apprentissage.
Ces modifications n’ont pas été observées dans la microglie de souris en bonne santé.
« Des changements dans l’expression des gènes dans les cellules microgliales pourraient perturber l’élagage des synapses, les connexions entre les cellules du cerveau, interférant avec la formation normale de nouvelles connexions qui devraient se produire par apprentissage », précisent les auteurs.
L’équipe a également étudié les modifications chimiques dans le cerveau de souris sans germe et a découvert que les concentrations de plusieurs métabolites associés à des troubles neuropsychiatriques, tels que la schizophrénie et l’autisme, étaient modifiées.
« La chimie du cerveau détermine essentiellement ce que nous ressentons et réagissons à notre environnement, et il est de plus en plus évident que les produits chimiques dérivés du microbiote intestinal jouent un rôle majeur », ajoutent les chercheurs.
Ensuite, les chercheurs ont tenté d’inverser les problèmes d’apprentissage chez les souris en restaurant leur microbiote intestinal à différents âges depuis la naissance.
« Nous étions surpris de pouvoir remédier aux déficits d’apprentissage chez les souris exemptes de germes, mais uniquement si nous intervenions immédiatement après la naissance, ce qui suggère que les signaux du microbiote intestinal sont nécessaires très tôt dans la vie. »

Des cibles prometteuses pour de nouveaux traitements
Enfin, cette découverte est intéressante à plus d’un titre, étant donné que de nombreux troubles psychiatriques associés à une maladie auto-immune sont associés à des problèmes au cours du développement précoce du cerveau.
L’axe intestin-cerveau a un impact sur chaque être humain, chaque jour de sa vie.
A ce jour, les scientifiques commencent à mieux comprendre l’influence de l’intestin sur des maladies aussi diverses que l’autisme, la maladie de Parkinson, le syndrome de stress post-traumatique (TSPT) et la dépression.
Ainsi, cette étude fournit un nouvel élément de compréhension sur le fonctionnement des mécanismes.
Ceci permettra éventuellement dans un futur proche d’identifier des cibles prometteuses qui pourraient être utilisées à l’avenir comme traitements pour l’homme.
© Blog Nutrition Santé – Jimmy Braun – Octobre 2019

Ce blog nutrition santé n’a pas vocation à remplacer votre relation avec votre médecin traitant. Les renseignements contenus sur le Blog Nutrition Santé sont tous rédigés avec des sources scientifiques et ne peuvent pas répondre à des questions médicales spécifiques, mais sont donnés à des fins purement informatives et complémentaires.
Lire la suite.
Sources externes
Coco Chu, Mitchell H. Murdock, Deqiang Jing, Tae Hyung Won, Hattie Chung, Adam M. Kressel, Tea Tsaava, Meghan E. Addorisio, Gregory G. Putzel, Lei Zhou, Nicholas J. Bessman, Ruirong Yang, Saya Moriyama, Christopher N. Parkhurst, Anfei Li, Heidi C. Meyer, Fei Teng, Sangeeta S. Chavan, Kevin J. Tracey, Aviv Regev, Frank C. Schroeder, Francis S. Lee, Conor Liston & David Artis. The microbiota regulate neuronal function and fear extinction learning. Nature, Octobre 2019, DOI: 10.1038/s41586-019-1644-y ; https://www.nature.com/articles/s41586-019-1644-y

