Notre microbiome intestinal influence le métabolisme à travers le système immunitaire. Une étude montre comment les « bonnes bactéries » nous maintiennent en bonne santé.
Le système immunitaire inné, notre première ligne de défense contre les infections bactériennes, a un rôle secondaire tout aussi important, il sert à affiner notre métabolisme.
La recherche nous dit que les bactéries commensales, appelées aussi « bonnes bactéries », qui peuplent nos intestins aident à réguler notre métabolisme. Une étude sur les mouches des fruits, publiée le 21 juin 2018 dans la revue Cell Metabolism, dévoile des informations surprenantes sur ce processus.

Microbiome intestinal et métabolisme
Dans l’intestin, les cellules digestives utilisent une voie immunitaire innée pour répondre aux bactéries nocives. Mais d’autres cellules intestinales, les cellules entéro-endocrines, utilisent la même voie, appelée IMD, pour répondre aux bonnes bactéries – en ajustant le métabolisme du corps au régime alimentaire et aux conditions intestinales.
Selon les auteurs, certaines voies immunitaires innées ne sont pas seulement pour l’immunité innée. « Les voies immunitaires innées écoutent aussi les « bonnes » bactéries – et réagissent métaboliquement. »

Syndrome métabolique, foie gras chez les mouches
Les chercheurs savaient d’après leurs recherches antérieures que les bactéries vivant dans les intestins des mouches fabriquent un acide gras à chaîne courte, l’acétate, essentiel au métabolisme des lipides et à la signalisation de l’insuline.
Les mouches sans bactéries dans leurs intestins — et par conséquent, sans d’acétate — ont accumulé de grosses gouttelettes dans leurs cellules digestives. Le laboratoire de Norbert Perrimon (PhD à la Harvard Medical School) avait précédemment trouvé des gouttelettes de graisse similaires chez les mouches dont les cellules entéro-endocrines manquaient de tachykinine, une protéine analogue à l’insuline importante dans la croissance, le métabolisme lipidique et la signalisation insulinique. Lorsqu’il y a un problème du traitement du glucose ou des lipides, les graisses se coincent dans ces gouttelettes dans des cellules qui ne sont pas conçues pour le stockage des graisses.
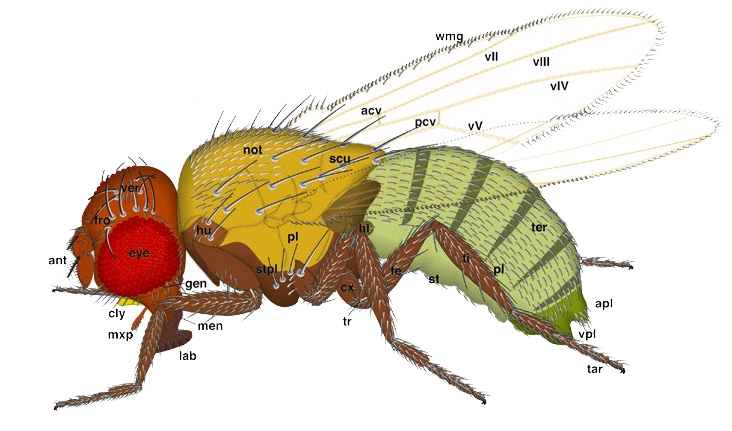
La nouvelle étude a encore utilisé des mouches des fruits, qui sont faciles à reproduire et à manipuler génétiquement, et ont des types de cellules dans leurs intestins un peu comme les humains. Lorsque les chercheurs ont examiné des mouches présentant des mutations dans la voie immunitaire innée de l’IMD (immune deficiency), ils ont de nouveau vu de grosses gouttelettes dans leurs intestins.
Les auteurs croient que ces grosses gouttelettes, qu’elles soient causées par la perte de bactéries intestinales, la perte de tachykinine ou la perte de la voie immunitaire innée, sont l’équivalent de la stéatose hépatique — qui est une affection caractérisée par l’accumulation de graisse dans les cellules du foie. Leur accumulation est un signe que le corps ne peut métaboliser correctement les glucides et les graisses. Essentiellement, les chercheurs pensent que ces mouches ont un syndrome métabolique, communément associé à l’obésité et au diabète de type 1. « Le syndrome métabolique est un problème de santé publique. Il se caractérise par l’association de plusieurs facteurs concourant à l’augmentation du risque cardio-vasculaire. »

Définir le rôle du système immunitaire dans le métabolisme
Comment sont liées les bactéries intestinales, le système immunitaire inné et le métabolisme ? Grâce à une série d’expériences, l’équipe de cette dernière recherche a commencé à démêler exactement comment les bactéries exercent leur influence métabolique.
Ces derniers ont montré que :
- La voie immunitaire innée stimule les cellules entéro-endocrines pour produire de la tachykinine.
- En l’absence de bactéries ou de leur produit de dégradation, l’acétate, aucune tachykinine n’est fabriquée.
- Lorsque des mouches exemptes de germes reçoivent de l’acétate, la voie immunitaire innée est réactivée et leur métabolisme se normalise.
- Un récepteur immunitaire inné spécifique sur les cellules entéro-endocrines (PGRP-LC) est nécessaire pour recevoir le signal de l’acétate.

Les auteurs indiquent qu’ils savent que les bactéries contrôlent notre métabolisme, mais que personne ne s’est rendu compte que les bactéries interagissaient avec les voies de signalisation immunitaire innée dans les cellules entéro-endocrines. Peut-être que ces voies sont vraiment un système qui permet aux cellules de reconnaître les bactéries pour différentes raisons.
Une interaction à deux volets
L’étude a également montré que l’activation de la voie immunitaire innée dans les cellules entéro-endocrines est essentielle pour la croissance et le développement normal des mouches. Lorsque les chercheurs ont inactivé la voie, ils ont eu des mouches retardées par la croissance. Nourrir les mouches en acétate ou réactiver directement la voie immunitaire innée les a fait grandir à nouveau.
Bien que les chercheurs souhaitent maintenant confirmer ces résultats dans un modèle de mammifère, l’étude décrit plus loin ce qui semble être une interaction à deux volets entre notre microbiome et notre métabolisme. De bonnes bactéries fermentent les nutriments dans notre alimentation et libèrent des acides gras à chaîne courte comme l’acétate, ce qui nous aide à optimiser notre utilisation et le stockage des nutriments.

Les « mauvaises » bactéries pathogènes font le contraire : elles consomment des acides gras, ce qui entrave le métabolisme sain. Un déséquilibre de notre microbiome intestinal a été lié à l’obésité et contribue parfois à la malnutrition.
Et parce que l’acétate est produit par la fermentation, les auteurs de l’étude spéculent que manger plus de glucides fermentescibles peut augmenter les niveaux d’acétate et favoriser un bon métabolisme. Ces aliments peuvent aider à contrer les déséquilibres de nos bactéries intestinales, tels que ceux causés par l’utilisation prolongée d’antibiotiques, suggèrent-ils. Les glucides fermentescibles, nommés aussi FODMAP, font l’objet de nombreuses publications et précautions, principalement dans le cadre du syndrome de l’intestin irritable. Dans cette dernière étude, les glucides fermentescibles (qui sont contenus essentiellement dans des aliments d’origine végétale tels que le blé, le seigle la pastèque, l’artichaut,…) reprennent une place privilégiée dans un régime alimentaire équilibré, et donc sans être totalement diabolisés.
© Blog Nutrition Santé – Jimmy Braun – Juin 2018
Ce blog nutrition santé n’a pas vocation à remplacer votre relation avec votre médecin traitant. Les renseignements contenus sur le Blog Nutrition Santé sont tous rédigés avec des sources scientifiques et ne peuvent pas répondre à des questions médicales spécifiques, mais sont donnés à des fins purement informatives et complémentaires. Lire la suite.
Sources externes
- « The Drosophila Immune Deficiency Pathway Modulates Enteroendocrine Function and Host Metabolism.« , Cell Metabolism, 2018, https://www.sciencedirect.com/science/article/pii/S1550413118303796?via%3Dihub ; DOI: 10.1016/j.cmet.2018.05.026
- « Immunité innée et inflammation », http://big.cea.fr/drf/big/Pages/BGE/GenChem/Immunite-innee-et-inflammation.aspx
- « Activation et régulation des voies Imd et JAK/STAT de Drosophile », http://www.afmb.univ-mrs.fr/activation-et-regulation-des-voies
- Photos © https://unsplash.com/search/photos/eating ; illustrations © 2018 Elsevier Inc. ; Adam Wong, PhD. Modified from Disease Models & Mechanisms. doi: 10.1242/dmm.023408.


Bonjour,
J’ai lu votre article sur le microbiote. Je conseille en premier lieu lors d’un rendez-vous de rééquilibrer PH sanguin et microbiote grâce à un élixir de thé lacto fermenté qui nourrit le microbiote. Les personnes atteintes d’arthrose ou de maladies inflammatoires en voient énormément de bénéfices. Je serai heureuse d’echanger avec vous sur les compléments alimentaires que je conseille. Produits 100% naturels, effets très rapides grâce aux synergies des composants, made in France
Joelleroy95@gmail.com